ชุดแยกอาร์เอ็นเอในเลือด
คำอธิบาย
ชุดอุปกรณ์นี้ใช้ spin column และสูตรที่พัฒนาโดยบริษัทของเรา ซึ่งสามารถสกัด RNA ทั้งหมดที่มีความบริสุทธิ์สูงและมีคุณภาพสูงได้อย่างมีประสิทธิภาพจากเลือดครบส่วนที่ต้านการแข็งตัวของเลือดชุดนี้มีเซลล์เม็ดเลือดแดง lysate (Buffer RCL) ซึ่งสามารถแยกเซลล์เม็ดเลือดแดงและรักษาเซลล์เม็ดเลือดขาวได้อย่างรวดเร็วและมีประสิทธิภาพคอลัมน์ทำความสะอาด DNA ที่มีประสิทธิภาพสามารถแยก supernatant และเซลล์ lysates และดูดซับและลบ DNA ของจีโนมได้อย่างง่ายดายการดำเนินการนั้นง่ายและประหยัดเวลาคอลัมน์เฉพาะ RNA สามารถผูก RNA ได้อย่างมีประสิทธิภาพ และด้วยสูตรเฉพาะ จึงสามารถประมวลผลตัวอย่างจำนวนมากได้ในเวลาเดียวกัน
ระบบทั้งหมดปราศจาก RNase ทำให้ RNA ที่แยกออกมาไม่สามารถย่อยสลายได้ระบบล้างบัฟเฟอร์ Buffer RW1 และ Buffer RW2 ทำให้ RNA ที่ได้รับปราศจากโปรตีน, DNA, ไอออนและมลพิษจากสารประกอบอินทรีย์
เนื้อหาชุด
| ชุดแยก RNA ในเลือดทั้งหมด | ||
| องค์ประกอบชุด | RE-04011 | RE-04013 |
| 50 ครั้ง | 200 ครั้ง | |
| บัฟเฟอร์ RCL (10×) | 52.5 มล | 210มล |
| บัฟเฟอร์ BRL1* | 30มล | 120มล |
| บัฟเฟอร์ BRL2 | 18มล | 66มล |
| บัฟเฟอร์ RW1* | 25มล | 100มล |
| บัฟเฟอร์ RW2 | 24มล | 96มล |
| RNase ฟรี ddH2 O | 10มล | 40มล |
| คอลัมน์ RNA เท่านั้น | 50 ชุด | 200 ชุด |
| คอลัมน์ทำความสะอาด DNA | 50 ชุด | 200 ชุด |
| คู่มือ | 1 สำเนา | 1 สำเนา |
คุณสมบัติและข้อดี
- ไม่ต้องกังวลเรื่องการเสื่อมของ RNAทั้งชุดปราศจาก RNase
- ง่าย—การดำเนินการทั้งหมดเสร็จสิ้นที่อุณหภูมิห้อง
-รวดเร็ว—ดำเนินการเสร็จภายใน 20 นาที
- ผลผลิต RNA สูง: คอลัมน์ RNA เท่านั้นและสูตรเฉพาะสามารถทำให้ RNA บริสุทธิ์ได้อย่างมีประสิทธิภาพ
-ปลอดภัย—ไม่ใช้สารอินทรีย์
- ความสามารถในการประมวลผลตัวอย่างขนาดใหญ่—สามารถประมวลผลตัวอย่างได้สูงสุด 200μl ในแต่ละครั้ง
- คุณภาพสูง — RNA ที่บริสุทธิ์มีความบริสุทธิ์สูง ปราศจากโปรตีนและสิ่งเจือปนอื่นๆ และสามารถตอบสนองการใช้งานเชิงทดลองขั้นปลายได้หลากหลาย
ชุดพารามิเตอร์
แอปพลิเคชันชุด:
เหมาะสำหรับการสกัดและทำให้บริสุทธิ์ RNA ทั้งหมดจากเลือดครบส่วนของสัตว์เลี้ยงลูกด้วยนม
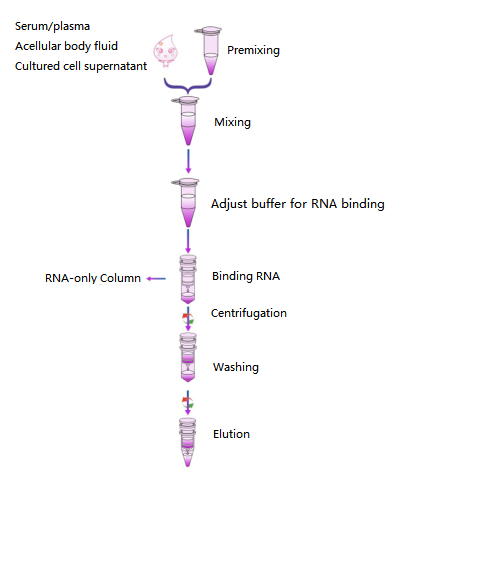
เวิร์กโฟลว์
สภาพการเก็บรักษา
ควรเก็บ Buffer RCL (10×) ไว้ที่ 2-8 ℃ ;ส่วนประกอบอื่นๆ ของชุดสามารถเก็บไว้ที่อุณหภูมิห้อง (15-25 ℃ ) ภายใต้สภาวะแห้ง และสามารถเก็บไว้ได้นาน 12 เดือนบัฟเฟอร์ BRL1 สามารถเก็บไว้ที่ 4 ℃ เป็นเวลา 1 เดือนหลังจากเติม β-mercaptoethanol (ทางเลือก)
หมายเหตุ: หากเก็บไว้ที่อุณหภูมิต่ำ สารละลายมีแนวโน้มที่จะตกตะกอนตรวจสอบให้แน่ใจว่าได้วางสารละลายในชุดไว้ที่อุณหภูมิห้องเป็นระยะเวลาหนึ่งก่อนใช้งานหากจำเป็น ให้อุ่นเครื่องในอ่างน้ำอุณหภูมิ 37° C เป็นเวลา 10 นาทีเพื่อให้ตะกอนละลาย และผสมให้เข้ากันก่อนใช้งาน
แนวทางการวิเคราะห์ปัญหา
The following is an analysis of the problems that might be encountered in the extraction of viral RNA. We wish it would be helpful to your experiment. In addition, for other experimental or technical problems other than operating instructions and problem analysis, we have dedicated technical support to help you. Contact us if you need at : 028-83361257or E-mail:Tech@foregene.com。
ไม่สามารถสกัด RNA ได้หรือผลผลิตของกรดนิวคลีอิกต่ำ
โดยปกติแล้วมีหลายปัจจัยที่ส่งผลต่อประสิทธิภาพการกู้คืน เช่น เนื้อหา RNA ตัวอย่าง วิธีการดำเนินการ ปริมาณการชะล้าง เป็นต้น。
การวิเคราะห์สาเหตุทั่วไป:
1. อ่างน้ำแข็งหรือการหมุนเหวี่ยงที่อุณหภูมิต่ำ (4 ° C) ระหว่างการทำงาน
คำแนะนำ: การทำงานที่อุณหภูมิห้อง (15-25 ° C) ห้ามแช่น้ำแข็งและหมุนเหวี่ยงอุณหภูมิต่ำ
2. การเก็บตัวอย่างที่ไม่เหมาะสมหรือเก็บตัวอย่างไว้นานเกินไป
คำแนะนำ: เก็บตัวอย่างที่อุณหภูมิ -80 °C หรือแช่แข็งในไนโตรเจนเหลว และหลีกเลี่ยงการใช้น้ำแข็งละลายซ้ำๆพยายามใช้ตัวอย่างที่เก็บใหม่สำหรับการสกัด RNA
3. การสลายตัวอย่างไม่เพียงพอ
คำแนะนำ: โปรดตรวจสอบให้แน่ใจว่าได้ผสมตัวอย่างและสารละลายทำงาน (ลิเนียร์อะคริลาไมด์) อย่างทั่วถึงและบ่มเป็นเวลา 10 นาทีที่อุณหภูมิห้อง (15-25 ° C)
4.เติมสารชะล้างไม่ถูกต้อง
คำแนะนำ: ตรวจสอบให้แน่ใจว่าได้เพิ่ม ddH2O ที่ปราศจาก RNase ที่กึ่งกลางของเมมเบรนของคอลัมน์การทำให้บริสุทธิ์
5.ปริมาณแอนไฮดรัสเอทานอลในบัฟเฟอร์ viRW2 ที่ไม่เหมาะสม
คำแนะนำ: โปรดปฏิบัติตามคำแนะนำ เติมเอทานอลปราศจากน้ำในปริมาณที่ถูกต้องลงใน Buffer viRW2 และผสมให้เข้ากันก่อนใช้ชุด。
6. การใช้ตัวอย่างที่ไม่เหมาะสม
คำแนะนำ: ตัวอย่าง 200µl ต่อ 500µl ของ Buffer viRLปริมาณตัวอย่างที่มากเกินไปจะส่งผลให้อัตราการสกัด RNA ลดลง
7.ปริมาณการชะที่ไม่เหมาะสมหรือการชะที่ไม่สมบูรณ์
คำแนะนำ: ปริมาตรชะล้างของคอลัมน์การทำให้บริสุทธิ์คือ 30-50μl;หากผลการชะไม่เป็นที่พอใจ แนะนำให้เติม RNase-Free ddH ที่อุ่นไว้ล่วงหน้า2O และยืดเวลาการวางที่อุณหภูมิห้อง เช่น 5-10 นาที
8.คอลัมน์การทำให้บริสุทธิ์มีเอธานอลตกค้างหลังจากล้างใน Buffer viRW2
คำแนะนำ: หากเอทานอลยังคงอยู่หลังจากล้างใน Buffer viRW2 และการปั่นแยกด้วยหลอดเปล่าเป็นเวลา 2 นาที คอลัมน์การทำให้บริสุทธิ์สามารถทิ้งไว้ที่อุณหภูมิห้องเป็นเวลา 5 นาทีหลังจากการปั่นแยกด้วยหลอดเปล่าเพื่อกำจัดเอทานอลที่เหลืออยู่ให้หมด
การสลายตัวของโมเลกุล RNA ที่บริสุทธิ์
คุณภาพของ RNA ที่บริสุทธิ์เกี่ยวข้องกับปัจจัยต่างๆ เช่น การเก็บตัวอย่าง การปนเปื้อนของ RNase และการทำงาน
การวิเคราะห์สาเหตุทั่วไป:
1.เก็บตัวอย่างไม่ทันเวลา
คำแนะนำ: หากตัวอย่างไม่ได้ใช้หลังการเก็บ โปรดเก็บไว้ที่อุณหภูมิ -80 ℃ หรือไนโตรเจนเหลวทันทีสำหรับการสกัดโมเลกุล RNA พยายามใช้ตัวอย่างที่เก็บมาใหม่ทุกครั้งที่ทำได้
2. เก็บตัวอย่างแช่แข็งและละลายซ้ำ
คำแนะนำ: หลีกเลี่ยงการแช่แข็งและละลายซ้ำ (ไม่เกิน 1 ครั้ง) ระหว่างการเก็บตัวอย่างและการเก็บรักษา มิฉะนั้น ผลผลิตของกรดนิวคลีอิกจะลดลง
3.RNase ถูกนำมาใช้ในห้องผ่าตัดหรือไม่มีการสวมถุงมือ หน้ากาก ฯลฯ แบบใช้แล้วทิ้ง
คำแนะนำ: การทดลองสกัดโมเลกุล RNA ทำได้ดีที่สุดในห้องผ่าตัด RNA ที่แยกจากกัน และทำความสะอาดโต๊ะทดลองก่อนการทดลองสวมถุงมือและหน้ากากแบบใช้แล้วทิ้งในระหว่างการทดลองเพื่อหลีกเลี่ยงการย่อยสลาย RNA ที่เกิดจากการนำ RNase
4. น้ำยาถูกปนเปื้อนโดย RNase ระหว่างการใช้งาน
คำแนะนำ: แทนที่ด้วย Viral RNA Isolation Kit ใหม่สำหรับการทดลองที่เกี่ยวข้อง
5.การปนเปื้อน RNase ของท่อปั่นแยก ทิปปิเปต ฯลฯ คำแนะนำ: ตรวจสอบให้แน่ใจว่าท่อปั่นแยก ทิปปิเปต และปิเปตทั้งหมดปลอดสาร RNase
โมเลกุล RNA ที่บริสุทธิ์ส่งผลต่อการทดลองขั้นปลาย
โมเลกุล RNA ที่ทำให้บริสุทธิ์โดยคอลัมน์การทำให้บริสุทธิ์จะส่งผลต่อการทดลองขั้นปลายหากมีไอออนของเกลือหรือโปรตีนมากเกินไป เช่น: การถอดความแบบย้อนกลับ, Northern Blot เป็นต้น。
1. มีเกลือไอออนเหลืออยู่ในโมเลกุล RNA ที่ถูกชะออก
คำแนะนำ: ตรวจสอบให้แน่ใจว่าได้เติมเอธานอลปราศจากน้ำในปริมาตรที่ถูกต้องใน Buffer viRW2 แล้ว และล้างคอลัมน์การทำให้บริสุทธิ์สองครั้งตามความเร็วการหมุนเหวี่ยงที่ถูกต้องในคู่มือการใช้งาน ถ้ายังมีเกลือไอออนเหลืออยู่ คุณสามารถเพิ่ม Buffer viRW2 ลงในคอลัมน์การทำให้บริสุทธิ์ และทิ้งไว้ที่อุณหภูมิห้องเป็นเวลา 5 นาทีจากนั้นทำการปั่นแยกเพื่อขจัดการปนเปื้อนของไอออนเกลือออกให้มากที่สุด
2. มีเอธานอลเหลืออยู่ในโมเลกุล RNA ที่ถูกชะออก
คำแนะนำ: เมื่อยืนยันว่าคอลัมน์การทำให้บริสุทธิ์ได้รับการล้างด้วย Buffer viRW2 แล้ว ให้ทำการปั่นเหวี่ยงท่อเปล่าตามความเร็วการหมุนเหวี่ยงในคู่มือการใช้งานหากยังมีเอทานอลเหลืออยู่ สามารถทิ้งไว้ 5 นาทีที่อุณหภูมิห้องหลังจากการปั่นแยกด้วยหลอดเปล่าเพื่อกำจัดเอทานอลที่เหลืออยู่ให้ได้มากที่สุด
คู่มือการใช้งาน:
คู่มือการใช้งานชุดแยก Viral RNA